近日�����,歌禮制藥宣布����,公司自主研發(fā)的丙肝藥物ASC18的臨床試驗申請獲得中國國家藥品監(jiān)督管理局(NMPA)的批準。ASC18是一款用于治療丙型肝炎的每日口服一次�����、每次一片的固定劑量復方制劑(Fixed Dose Combination, FDC)���。這是歌禮制藥研發(fā)的又一款直接抗病毒丙肝治療創(chuàng)新藥�����。公司的首款丙肝藥戈諾衛(wèi)已于2018年在中國獲批上市���;第二款丙肝藥拉維達韋的上市申請已獲受理����,并被納入優(yōu)先評審����。
歌禮是一家創(chuàng)新研發(fā)驅動型生物科技公司,致力于解決抗病毒�����、癌癥及脂肪肝疾病三大治療領域中尚未被滿足的醫(yī)療需求���。該公司于2018年已在香港證券交易所上市�,且目前已經有兩款上市產品��,其中一款是用于丙肝治療的直接抗病毒藥物戈諾衛(wèi)����,也是首款由中國本土企業(yè)研發(fā)上市的直接抗病毒丙肝創(chuàng)新藥,另一款則是歌禮和與羅氏合作的用于乙肝�、丙肝治療的具有良好市場基礎的長效干擾素派羅欣。除此之外,歌禮的研發(fā)管線包括處于不同臨床開發(fā)階段的抗體免疫療法�����、全球首創(chuàng)或同類最佳的小分子藥物和siRNA藥物�。進入2019年,歌禮不斷取得新進展:2019年3月�,其用于治療丙型肝炎的NS5B核苷類聚合酶抑制劑ASC21的臨床試驗申請獲得NMPA批準。此次�����,丙肝治療在研藥物ASC18的臨床試驗申請也獲得批準����,是歌禮2019年在研發(fā)方面的又一新進展�。
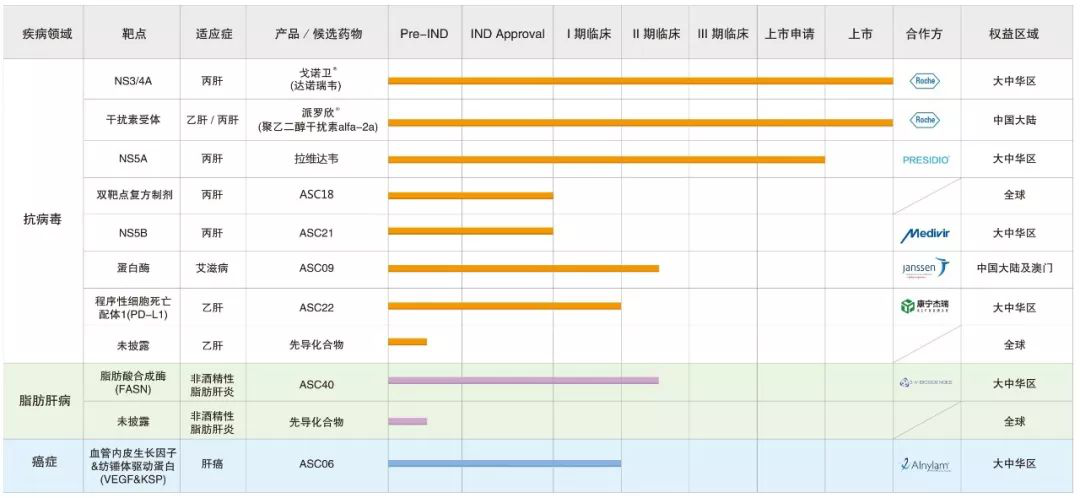
▲歌禮制藥研發(fā)管線(圖片來源:歌禮官網)
歌禮制藥創(chuàng)始人、董事長兼首席執(zhí)行官吳勁梓博士說:“歌禮正在按照既定計劃完成2019年的研發(fā)里程碑���,我們想再次強調公司的基本面無變化且非常強勁�。管理團隊有信心實現公司2019年的目標�,包括研發(fā)、醫(yī)保準入�����,以及引進、收購處于臨床階段和已商業(yè)化的項目���,同時進一步提升本公司財務業(yè)績表現����。管理團隊也對公司2020年及今后的發(fā)展前景持樂觀態(tài)度����。”

▲歌禮公司創(chuàng)始人、董事長兼首席執(zhí)行官吳勁梓博士(圖片來源:歌禮官網)
他還表示:“作為一家擁有兩個上市產品(戈諾衛(wèi)和派羅欣)的創(chuàng)新研發(fā)驅動型生物科技公司��,在公司業(yè)務的所有關鍵職能崗位�,我們成功地吸引了來自各跨國公司的人才。在成功保留和培養(yǎng)發(fā)展眾多人才的同時�����,公司持續(xù)吸引著全球的跨國公司和生物技術行業(yè)特別是在研發(fā)和商業(yè)化方面的高層次人才���。”





